Par Pascal Philippot
Dans cet article, Pascal Philippot [1], discute des plus anciennes traces d’eau liquide et matière organique sur Terre.
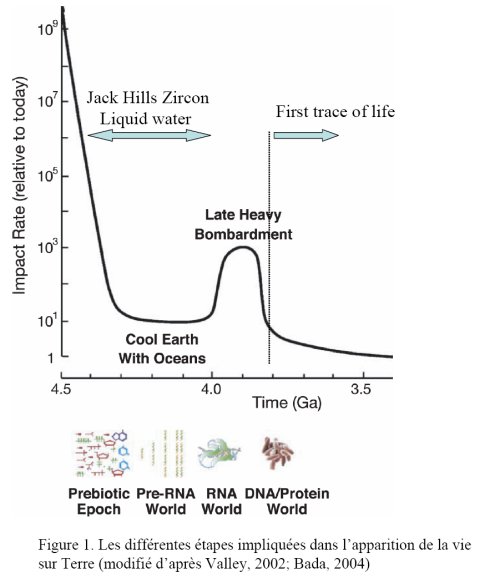
Durant la phase finale d’accrétion de la Terre et tout particulièrement durant la période qui a suivi la formation de la lune vers 4,51 milliards d’années (4,51 Ga), il est couramment admis que la Terre était couverte de roches en fusion, ou océans de magma (Sleep et al., 2001). Dans ces conditions, l’eau devait être présente sous forme de vapeur dans l’atmosphère et aucun composé organique nécessaire à la fabrication des briques élémentaires de la vie n’aurait pu subsister. Bien que nous ne connaissons pas de roches plus vieilles que 4,04 milliards d’années pour tester cette hypothèse (Bowring et Williams, 1999), les teneurs en éléments traces des zircons de Jack Hills (Australie occidentale) datés entre 4,4 et 4,0 Ga (Wilde et al., 2001) indiquent des températures de cristallisation de l’ordre de 700 °C, similaires aux conditions de formation des zircons dans les magmas granitiques actuels (Watson et Harrison, 2005). Les rapports isotopiques de l’oxygène de ces mêmes zircons montrent des valeurs de 6 à 9 ‰ caractéristiques de la fusion de roches préalablement altérées par des fluides de basses températures (Mojzsis et al., 2001 ; Valley et al., 2002). Cela suggère qu’un mécanisme régulateur de cristallisation des zircons était déjà en place dans la proto-croûte Hadéenne (période de l’histoire de la Terre comprise entre 4,6 et 4,0 Ga), et que la température à la surface de la Terre avait suffisamment baissé pour permettre la condensation d’eau liquide environ 200 million d’années après sa formation. Si l’on admet que l’essentiel de l’eau terrestre dérive du dégazage de minéraux hydratés initialement présents dans le manteau terrestre et en moindre partie du bombardement d’astéroïdes et de comètes (Dauphas et al., 2000), cela implique que des volumes d’eau similaires aux volumes des océans actuels étaient présents à la surface de la Terre pendant des périodes relativement longues entre 4,4 et 4,0 Ga. Si l’on en croit l’enregistrement des cratères lunaires, cette période est également une période d’accalmie en terme de bombardement météoritique (Ryder, 2003), ce qui aurait pu s’accompagner de la préservation de composés organiques d’origines diverses et ainsi permettre d’amorcer les premières étapes de la vie (Figure 1).
Dans cet exposé je présente les connaissances sur la composition, la salinité, la température et l’état redox de l’océan précambrien et je discute succinctement les relations souvent équivoques entre traces de vie fossiles, contraintes géologiques et interprétations environnementales.
.
.
État redox de l’océan primitif
Le schéma classique de l’évolution de l’état redox de l’océan primitif est le découpage en deux grandes périodes de durée équivalente. Une période anoxique entre, disons, 4 et 2 milliards d’années, suivie par une période riche en oxygène, type « océan moderne », depuis 2 milliards d’années jusqu’à nos jours (Holland, 1984 ; voir Ohmoto, 1993 pour une controverse). L’argument majeur en faveur de l’apparition d’un océan oxique vers 2 milliards d’années est fondé sur la disparition des fameux Banded Iron Formations (BIF), c’est-à-dire ces masses gigantesques de sédiments riches en fer et silice qui jalonnent les cratons précambriens et dont le dépôt nécessite l’accumulation et le transport de fer ferreux (Fe2+) d’origine hydrothermale dans des eaux profondes anoxiques. L’oxydation de l’océan se serait traduite par la production de fer ferrique (Fe3+) qui aurait précipité rapidement sous forme de Fe-hydroxyde, limitant ainsi l’accumulation de fer et la formation des BIF.
La découverte de fractionnement des isotopes du soufre indépendant de la masse (MIF) des sulfures et sulfates sédimentaires et hydrothermaux archéens a fourni la preuve difficilement contestable en faveur d’une atmosphère archéenne réductrice (Farquhar et al., 2000 ; Farquhar et Wing, 2003 ; Figure 2). D’après ces auteurs, la signature MIF des isotopes du soufre dans les roches archéennes est liée à des réactions photochimiques de composés volcaniques soufrés (H2S, SO2) induites par le rayonnement UV solaire dans une atmosphère dépourvue d’écran d’ozone protecteur. L’absence de signature MIF dans les roches plus jeunes que 2 milliards d’années a été attribuée à l’augmentation des teneurs en oxygène de l’atmosphère (environ 10-2 les teneurs actuelles) et à la formation d’un écran d’ozone.
.
.
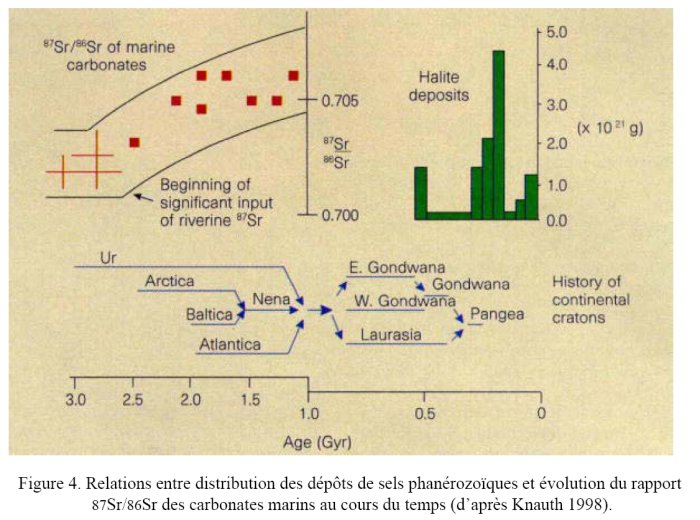
L’augmentation des teneurs en oxygène de l’atmosphère vers 2 milliards d’années n’implique pas nécessairement l’oxydation généralisée de l’océan primitif. Du fait que la solubilité des sulfures soit également très faible dans l’eau de mer, une hypothèse récemment avancée par Canfield (1998) pour expliquer la disparition des BIF est la formation d’un océan « soufré », c’est-à-dire très réducteur, et ce indépendamment de l’augmentation de l’oxygène atmosphérique. Ainsi, l’océan anoxique a pu persister durant tout ou partie du Protérozoïque (2,5 à 0,55 Ga), probablement sous la forme d’un environnement stratifié caractérisé par un niveau profond réducteur et soufré et une couche superficielle progressivement enrichie en composés oxydés (sulfate) issus vraisemblablement de l’altération des continents progressivement émergés comme l’indique l’évolution des rapports 87Sr/86Sr des carbonates marins (voir figure 4). Un tel environnement riche en H2S se serait traduit par une limitation de l’apport en métaux bio-essentiels tels que Fe, Mo et en moindre partie Cu, Zn et Cd, affectant ainsi la productivité primaire et limitant le développement de la diversité eucaryote. Cette étape Protérozoïque peut-être perçue comme une période de « transition bio-inorganique », où se seraient tissés les liens de causalité entre contexte environnemental et évolution biologique (Anbar et Knoll, 2002 ; Shen et al., 2003 ; Rouxel et al., 2005).
Température de l’océan primitif
L’occurrence généralisée de basaltes en coussin, de stratifications entrecroisées, de structures stromatoliques dès 3,5 Ga indique que de l’eau libre de moins de 100°C était probablement disponible en abondance durant l’Archéen Inférieur. Les cherts composés de quartz microcristallin sont très abondants dans les roches sédimentaires précambriennes. Ces cherts se forment en général lors de la stabilisation des carbonates sous forme de silice amorphe (opale) métastable qui, sous l’action des eaux interstitielles diagénétiques ou hydrothermales, va se dissoudre et reprécipiter sous forme de cherts. Dans les échantillons phanérozoïques, l’opale primaire est en général biogénique et associée à l’activité des diatomées et des radiolaires. Dans les échantillons précambriens, la silice est d’origine inorganique et dérive soit directement de l’océan saturé en silice soit de fluides hydrothermaux ou météoriques qui lessivent le bâti sédimentaire ou volcanique (Knauth, 1994). Le quartz est un des minéral les plus résistants à l’altération isotopique et les cherts sont des roches très peu perméables et relativement peu sensibles aux processus de dissolution-recristallisation si communs dans les roches carbonatées. Pour cette raison, et en faisant l’hypothèse forte que la signature isotopique de l’oxygène n’est pas affectée par la recristallisation de l’opale sous forme de cherts ni par les processus de silicification secondaire extrêmement courant à l’archéen, la composition isotopique des cherts a souvent été utilisée pour caractériser la température de l’eau de mer en équilibre avec la silice amorphe (Perry, 1967 ; Knauth et Epstein, 1976 ; Knauth et Lowe, 1978).
La figure (3) indique que les cherts précambriens montrent un enrichissement progressif en isotope 18O au cours des temps géologiques attribué à un refroidissement climatique progressif de la Terre. La différence d’environ 10‰ entre les cherts phanérozoïques et archéens a été attribuée à une différence de température de l’ordre de 40°C, les roches archéennes ayant équilibré dans un environnement plus chaud que leurs équivalents phanérozoïques (Knauth et Lowe, 2003 ; Knauth 2005). Bien que les données soient encore très partielles, en particulier en ce qui concerne les transitions Archéen-Protérozoïque et Protérozoïque-Phanérozoïque, le profil général suggère que l’océan archéen était sensiblement plus chaud que l’océan actuel (Perry, 1967).
.
.
Salinité de l’océan primitif
Les teneurs en sels et l’évolution de la salinité de l’océan au cours des temps géologiques ont été estimées de deux manières. De manière indirecte, en faisant l’inventaire des dépôts de sels connus dans l’enregistrement géologique, ce qui a permis d’estimer la salinité globale de l’océan primitif avant la formation des premiers continents émergés. De manière directe, en déterminant les rapports et les concentrations élémentaires dans des fluides piégées en inclusions dans des minéraux de roches sédimentaires et hydrothermales. En particulier, la rapport Cl/Br est considéré comme conservatif dans la plupart des environnements géologiques et est ainsi très utilisé pour reconstruire l’origine des fluides (météorique, océanique, magmatique) dans l’enregistrement géologique.
La formation épisodique de « géants salins » sur les continents émergés ou dans des environnements océaniques clos et leur remobilisation par érosion a du s’accompagner de fortes variations de salinité de l’océan au cours des temps géologiques (Knauth, 1998). Ces variations sont difficilement contraignables car elles dépendent de la fréquence de la formation et du lessivage des dépôts de sels. La figure 4 montre que 40% des dépôts évaporitiques phanérozoïques se sont formés dans l’intervalle 180-250 Ma et durant la transition Néoprotérozoïque-Cambrien. En supposant que tout le chlore a dégazé avec l’eau durant la différenciation terrestre (Holland, 1976), la salinité initiale de l’océan primitif calculée en prenant en compte les dépôts évaporitiques phanérozoïques et les saumures piégées dans les cratons continentaux a été estimée à environ 2 fois la salinité des océans actuels, soit environ 7 à 8% poids équivalent NaCl (Knauth, 1998 ; 2005).
.
.
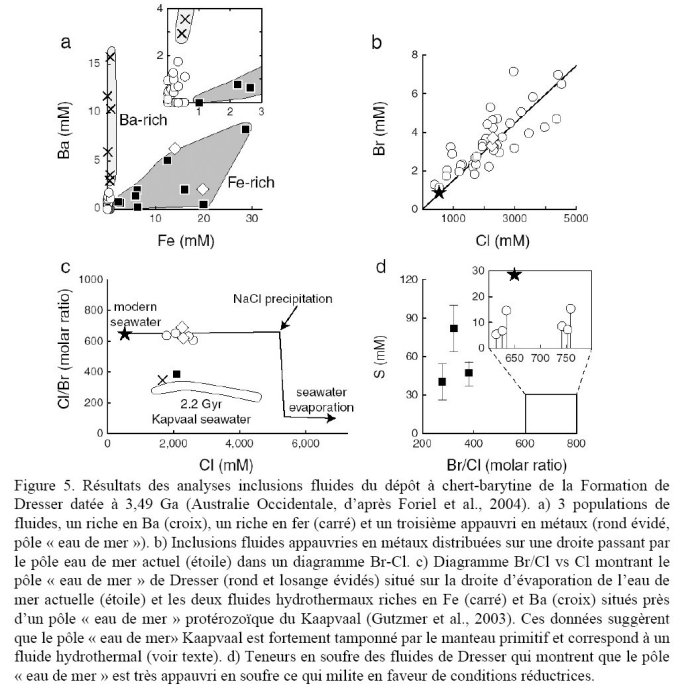
L’analyse d’inclusions fluides individuelles préservées dans des ségrégations à quartz et carbonate dans des cœurs de basaltes en coussin de la formation à chert-barytine de Dresser datée à 3,49 Ga (Australie Occidentale) a permis d’identifier une génération d’inclusions fluides présentant le même rapport Cl/Br (630) que l’eau de mer actuelle (649) mais une salinité 3 à 4 fois supérieure (Foriel et al., 2004 ; Figure 5). Deux autres types de fluides, l’un riche en fer et soufre et l’autre en barium sont également présents dans les échantillons étudiés. Ces deux populations montrent un rapport Cl/Br (350-390) proche de la valeur de la Terre globale (420), c’est-à-dire le rapport primitif issu du dégazage initial et ont été interprétées comme des témoins de fluides hydrothermaux tamponnés par un pôle magmatique. Ces valeurs Cl/Br hydrothermales sont similaires aux valeurs moyennes de « l’eau de mer » protérozoïque telle qu’elle a été définie dans le craton de Kaapvaal à 2,2 Ga (Gutzmer et al., 2003), ce qui implique soit que « l’eau de mer » du Kaapvaal était largement tamponnée par des fluides hydrothermaux ou que les analyses globales dont sont extrait ce rapport n’ont pas permis de distinguer le « vrai pôle eau de mer » protérozoïque. La salinité estimée dans la formation de Dresser par Foriel et al., (2004) est comparable aux estimations faites dans les formations d’Isua à 3,8 Ga (Groenland, Appel et al., 2001), de Barberton à 3,2 Ga (Afrique du Sud ; Channer et al., 1997 ; de Ronde et al., 1997 ; mais voir Lowe et Byerly, 2003, pour une controverse), et de l’Abitibi à 2,7 Ga (Canada ; Weiershaüser et Spooner, 2005). Ces dernières données ont été obtenues par microthermométrie et ne permettent pas de rendre compte des teneurs en Br et éléments traces et donc de faire la distinction entre fluides hydrothermaux et pôle « eau de mer ». Elles convergent cependant en faveur de l’existence d’un océan précambrien nettement plus salin que l’océan actuel, en accord avec les calculs de bilan de masse.
.
.
Traces de vie fossile, contextes géologiques et interprétations environnementales
L’enracinement profond dans l’arbre phylogénétique des microorganismes thermophiles et hyperthermophiles et de certains groupes de sulfato-réductrices a conduit à la notion d’une origine hydrothermale de la vie fondée sur le cycle du soufre, hypothèse en partie étayée par la gamme relativement étendue des valeurs delta34S de pyrites microcristallines dans la Formation de Dresser à 3,49 Ga (Australie Occidentale ; Shen et al., 2001 ; Shen et Buick, 2003). Au-delà, le lien entre domaine phylogénétique et morphologie des microfossiles ou signature isotopique d’élément biologique comme le carbone ou l’azote reste largement spéculatif. Ainsi, les forts appauvrissement en 13C attribués au graphite des roches archéennes du Groenland (3,8 Ga) et longtemps interprétés comme le témoignage de vie le plus primitif (Mojzsis et al., 1996 ; Ueno et al., 2002), sont aujourd’hui attribués en partie à la décomposition à haute température de carbonate de fer sous forme de magnétite et graphite (Van Zuilen et al., 2002). Les fameuses traces de cyanobactéries fossiles de la Formation Apex (Australie Occidentale) qui permettaient de faire remonter à 3,5 Ga les premières traces de photosynthèse oxique (Schopf 1983 ; Schopf et al., 2002) sont maintenant interprétés comme des condensats inorganiques polymérisés à faible température pour former des produits « kérogéneux » (Brasier et al., 2002 ; Garcia Ruiz et al., 2003).
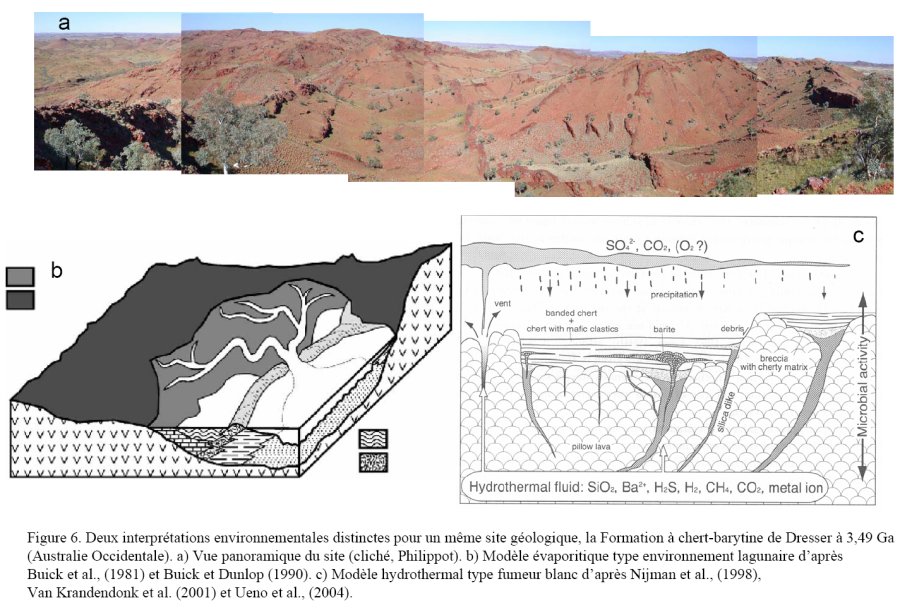
Peut-être plus surprenant est de constater que les interprétations du contexte géologique dans lequel s’inscrivent ces débats sont tout aussi controversées. Partie des roches amphibolitisées du Groenland longtemps considérées comme des témoins de sédiments métamorphisés (type Banded Iron Formation) sont interprétées aujourd’hui comme des roches ultramafiques, c’est-à-dire mantelliques, altérées et métamorphisées (Fedo et Whitehouse, 2002). De la même manière, la formation de Dresser, pourtant une des mieux étayées en terme de marqueurs morphologiques (structures stromatolitiques et filaments organiques fossilisés ; Buick et al., 1981 ; Buick et Dunlop, 1990 ; Ueno et al., 2004), chimiques (Terabayashi et al., 2003 ; Foriel et al., 2004) et isotopiques (S, C, N ; Beaumont et Robert, 1999 ; Pinti et al., 2001 ; Shen et al., 2001 ; Shen et Buick 2003 ; Ueno et al., 2004) est interprétée soit comme un environnement évaporitique carbonaté peu profond de type lagon (Buick et al., 1981 ; Buick et Dunlop, 1990 ; Shen et Buick, 2003) soit comme un système hydrothermal de basse température, type fumeur blanc, alimenté par des venues massives de fluides hydrothermaux le long de veines de cherts noirs et de sulfates-sulfures (Nijman et al. 1998 ; Van Kranendonk et al., 2000 ; Pirajno and Van Kranendonk, 2005 ; Figure 6). Les observations morphologiques et les données isotopiques du soufre sont interprétables dans les deux contextes géologiques par contre celles du carbone, de l’azote et les analyses inclusions fluides sont en meilleure adéquation avec un environnement hydrothermal. La vérité est à rechercher probablement entre ces deux extrêmes, suggérant que le contexte environnemental primitif a pu, lui aussi, évoluer au cours des temps géologiques avant d’aboutir au niveau de finition et de complexité tel que nous le connaissons actuellement.
.
.
Références Bibliographiques
Anbar, A. D. and A. H. Knoll (2002). « Proterozoic ocean chemistry and evolution : a bioinorganic bridge. » Science 297 : 1137-1142.
Appel, P. W. U., H. R. Rollinson, et al. (2001). « Remnants of an Early Archaean (>3.75 Ga) sea-floor hydrothermal system in the Isua Greenstone Belt. » Precambrian Research 112 : 27-49.
Awramik, S. M., J. W. Schopf, et al. (1983). « Filamentous fossil bacteria 3.5 109 years old from the Archean of Western Australia. » Precambrian Research 20(2-4) : 357-374. Bada, J. L. (2004). « How life began on Earth : a status report. » ESPL 226 : 1-15.
Beaumont, V. and F. Robert (1999). « Nitrogen isotope ratios of kerogens in Precambrian cherts ; a record of the evolution of atmosphere chemistry ? » Precambrian Research 96(1-2) : 63-82.
Brasier, M. D., O. R. Green, et al. (2002). « Questioning the evidence for Earth’s oldest fossils. » Nature 416 : 76-81.
Buick, R. and J. S. R. Dunlop (1990). « Evaporitic sediments of early Archaean age from the Warrawoona Group, North Pole, Western Australia. » Sedimentology 37 : 247-277.
Buick, R., J. S. R. Dunlop, et al. (1981). « Stromatolite recognition in ancient rocks : an appraisal of irregularly laminated structures in an Early Archaean chert-barite unit from North Pole, Western Australia. » Alcheringa 5 : 161-181.
Canfield, D. E. (1998). « A new model for Proterozoic ocean chemistry. » Nature 396 : 450-453.
Channer, D. M. D., E. J. De Ronde, et al. (1997). « The Cl—Br—I- composition of 3.23 Ga modified seawater : implications for the geological evolution of ocean halide chemistry. » Earth and Planetary Science Letters 150 : 325-335.
Dauphas, N. F., F. Robert, et al. (2000). « The late asteroidal and comatery bombardment of Earth as recorded in water deuterium to protium ratio. » Icarus 148 : 508-512.
De Ronde, E. J., D. M. D. Channer, et al. (1997). « Fluid chemistry of Archean seafloor hydrothermal vents : Implications for the composition of circa 3.2 Ga seawater. » Geochimica et Cosmochimica Acta 61 : 4025-4042.
Farquhar, J., H. Bao, et al. (2000). « Atmospheric Influence of Earth’s Earliest Sulfur Cycle. » Science 289 : 756.
Farquhar, J. and B. A. Wing (2003). « Multiple sulfur isotopes and the evolution of the atmosphere. » Earth and Planetary Science Letters 213 : 1-13.
Fedo, C. M. and M. J. Whitehouse (2002). « Metasomatic Origin of Quartz-Pyroxene Rock, Akilia, Greenland, and Implications for Earth’s Earliest Life. » Science 296 : 1448-1452.
Foriel, J., P. Philippot, et al. (2004). « Low sulphate concentration and biological control of the Cl/Br ratio in the Early Archaean ocean. » Earth and Planetary Science Letters 228 : 451-463.
Furnes, H., N. R. Banerjee, et al. (2004). « Early life recorded in Archean pillow lavas. » Science 304 : 578-581.
Garcia-Ruiz, J. M., S. T. Hyde, et al. (2003). « Self-assembled silica-carbonate stryctyres and detection of ancient microfossils. » Science 302 : 1194-1197.
Gutzmer, J., D. A. Banks, et al. (2003). « Ancient sub-seafloor alteration of basaltic andesites of the Ongeluk Formation, South Africa : implications for the chemistry of Ancient sub-seafloor alteration of basaltic andesites of the Ongeluk Formation. » Chemical Geology 201 : 37-53.
Holland, H. D. (1976). The evolution of seawater. The early history of the Earth. B. F. Windley, John Wiley & Sons, New York, N. Y., United States (USA) : 559-567.
Holland, H. D. (1984). The chemical evolution of the atmosphere and oceans. Princeton, Princeton University Press.
Knauth, L. P. (1998). « Salinity history of the Earth’s early ocean. » Nature 395 : 554-555.
Knauth, L. P. (2005). « Temperature and Salinity history of the Precambrian ocean : implications for the course of microbial evolution. » Palaeogeography Palaeoclimatology Palaeoecology 219 : 53-69.
Knauth, L. P. and S. Epstein (1976). « Hydrogen and oxygen isotope ratios in nodular and bedded cherts. » Geochimica et Cosmochimica Acta 40 : 1095-1108.
Knauth, L. P. and D. R. Lowe (1978). « Oxygen isotope geochemistry of cherts from the Onverwacht Group (3.4 b.y.), Transwaal, South Africa, with implications for secular variations in the isotopic composition of cherts. » Earth and Planetary Science Letters 41 : 209-222.
Knauth, L. P. and D. R. Lowe (2003). « High Archaean climatic temperature inferred from oxygen isotope geochemistry of cherts in the 3.5 Ga Swaziland Supergroup, South Africa. » GSA bulletin 115(5) : 566-580.
Lowe, D. R. and G. R. Byerly (2003). « Ironstone pods in the Archean Barberton greenstone belt, South Africa : Earth’s oldest seafloor hydrothermal vents reinterpreted as Quaternary subaerial springs. » Geology 31(10) : 909-912.
Mojzsis, S. J., G. Arrhenius, et al. (1996). « Evidence for life on Earth before 3,800 million years ago. » Nature 384(6604) : 55-59.
Mojzsis, S. J., T. M. Harrison, et al. (2001). « Oxygen-isotope evidence from ancient zircons for liquid water at the Earth’s surface 4,300 Myr ago. » Nature 409 : 178-181.
Nijman, W., K. C. H. De Bruijne, et al. (1998). « Growth fault control of early Archaean cherts, barite mounds and chert-barite veins, North Pole Dome, eastern Pilbara, Western Australia. » Precambrian Research 88 : 25-52.
Ohmoto, H., T. Kakegawa, et al. (1993). « 3.4-Billion-Year-Old Biogenic Pyrites from Barberton, South Africa : Sulfur Isotope Evidence. » Science 262(5133) : 555-557.
Pinti, D., K. Hashizume, et al. (2001). « Nitrogen and argon signatures in 3.8 to 2.8 Ga metasediments ; clues on the chemical state of the Archean ocean and the deep biosphere. » GCA 65(14) : 2301-2315.
Pinti, D. L., K. Hashizume, et al. (2003). « Nitrogen quest in Archean metasediments of Pilbara, Australia. » GCA 67((18) Suppl. 1) : A379.
Pirajno, F. and M. J. Van Kranendonk (2005). « Review of hydrothermal processes ans systems ob Earth and implications for Martian analogues. » Australian J. Earth Sci. 52 : 329-351.
Rosing, M. (1999). « 13C-depleted carbon microparticles in >3700-Ma sea-floor sedimentary rocks from West Greenland. » Science 283(5402) : 674-676.
Rouxel, O. J., A. Bekker, et al. (2005). « Iron isotope constraints on the Archaean and Paleoproterozoic ocean redox state. » Science 307 : 1088-1091.
Ryder, G. (2003). « Bombardment of the Hadean Earth : Wholesome or Deleterious ? » Astrobiology 3(1) : 3-6.
Schopf, J. W., A. B. Kudryavtsev, et al. (2002). « Laser-Raman imagery of Earth’s earliest fossils. » Nature 416 : 73-76.
Schopf, J. W. and M. R. Walter (1983). Archean microfossils : New evidences of ancient microbes. Earth’s Earliest Biosphere : Its Origins and Evolution. J. W. Schopf. Princeton, NJ, Princeton University Press : 214-239.
Shen, Y. and R. Buick (2003). « The antiquity of microbial sulfate reduction. » Earth-Science Reviews 64 : 243-272.
Shen, Y., R. Buick, et al. (2001). « Isotopic evidence for microbial sulphate reduction in the early Archaean era. » Nature 410 : 77-81.
Shen, Y., A. H. Knoll, et al. (2003). « Evidence for low sulphate and anoxia in a mid-Proterozoic marine basin. » Nature 423 : 632-635.
Sleep, N. H., K. J. Zahnle, et al. (2001). « Initiation of element surface conditions on the earliest Earth. » Proc. Nat. Acad. Sci. USA 98 : 3666-3672.
Terabayashi, M., Y. Masada, et al. (2003). « Archean ocean-floor metamorphism in the North Pole area, Pilbara Craton, Western Australia. » Precambrian Research 127(1-3) : 167-180.
Ueno, Y., H. Yoshioka, et al. (2004). « Carbon isotopes and petrography of kerogens in 3.5-Ga hydrothermal silica dikes in the North Pole area, Western Australia. » Geochimica et Cosmochimica Acta 68(3) : 573-589.
Ueno, Y., H. Yurimoto, et al. (2002). « Ion microprobe analysis of graphite from ca. 3.8 Ga metasediments, Isua supracrustal belt, West Greenland : Relationship between metamorphism and carbon isotopic composition. » GCA : 1257-1268.
Valley, J. W., W. H. Peck, et al. (2002). « A cool early Earth. » Geology 30 : 351-354.
Van Kranendonk, M. J., A. H. Hickman, et al. (2001). Archaean geology of the East Pilbara Granite-Greenstone Terrane, Western Australia – a field guide, Geol. Surv. of Western Aust., vol 9, 134pp.
van Zuilen, M. A., A. Lepland, et al. (2002). « Reassessing the evidence for the earliest traces of life. » Nature 418 : 627-630.
Weiershaüser, L. and E. T. C. Spooner (2005). « Seafloor hydrothermal fluids, Ben Nevis area, Abitibi Greenstone Belt : implications for Archaean ( 2.7 Ga) seawater properties. » Precambrian Research 138 : 89-123.
Wilde, S. A., J. W. Valley, et al. (2001). « Evidence from detrital zircons for the existence of continental crust and oceans on the Earth 4.4 Gyr ago. » Nature 409 : 175-178.
___________________________________________
[1] Pascal Philippot est Chargé de Recherche au CNRS, au Laboratoire Biogéosphère Actuelle et Primitive,Institut de Physique du Globe de Paris







Aucun commentaire sur l'article Systèmes hydrothermaux et sédiments Archéens : traces des premiers océans et des premières matières organiques